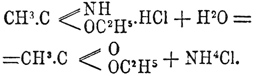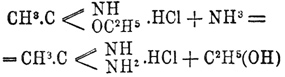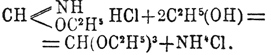Имидоэфиры
Энциклопедия Брокгауза Ф.А. и Ефрона И.А. (1890 - 1916гг.) Статьи для написания рефератов, курсовых работ, научные статьи, биографии (118447 статей и 6000 рисунков).
|
|
| А | Б | В | Г | Д | Е | Ё | Ж | З | И | Й | К | Л | М | Н | О | П | Р | С | Т | У | Ф | Х | Ц | Ч | Ш | Щ | Ы | Э | Ю | Я | A | B | C | D | E | F | G | H | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | Z |
| И | ИА | ИБ | ИВ | ИГ | ИД | ИЕ | ИЖ | ИЗ | ИИ | ИЙ | ИК | ИЛ | ИМ | ИН | ИО | ИП | ИР | ИС | ИТ | ИУ | ИФ | ИХ | ИЦ | ИЧ | ИШ | ИЩ | ИЮ | ИЯ |
| ИМА |
| ИМБ |
| ИМГ |
| ИМЕ |
| ИМЗ |
| ИМИ |
| ИММ |
| ИМН |
| ИМО |
| ИМП |
| ИМР |
| ИМУ |
| ИМШ |
| ИМЯ |
Имидоэфиры (хим.) — представляют производные имидокислот (см.) и изображаются следующими формулами строения: 1) для Имидоэфиры одноосновных кислот 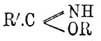 и 2) для Имидоэфиры двуосновных кислот
и 2) для Имидоэфиры двуосновных кислот 
Имидоэфиры открыты и исследованы Пиннером (1878-92). Они получаются действием хлористоводородного газа на разбавленные эфиром смеси частичных количеств соответствующих нитрилов (см.) и спиртов при охлаждении. При этом сперва образуются хлоргидраты хлорамидоэфиров, которые уже при высушивании разлагаются с образованием хлоргидратов Имидоэфиры Последние при осторожном действии щелочей на холоду выделяют свободные Имидоэфиры Следующие уравнения изображают получение ацетимидоэтилового эфира:
CH3 CN [ацетонитрил] + C 2H5 (OH) [этил. спирт] + 2HCl = CH 3C(NH2)(OC2H5)Cl∙HCl = CH3C(NH)(OC2H5)HCl + HCl;
CH3C(NH)(OC2H5)HCl + NaHO = CH3C(NH)(OC2H5) + NaCl + H2O.
В настоящее время Пиннером получено таким путем довольно большое число представителей этого класса соединений, как из жирного, так и из ароматического ряда. Имидоэфиры одноосновных кислот представляют большей частью маслообразные пахучие жидкости; Имидоэфиры кислот двухосновных кристалличны. Это — вещества весьма непрочные, щелочами и водными кислотами легко разлагаемые, с аммиаком дающие амидины, напр.:
CH3C(NH)(OC2H5) + NH3 = CH3C(NH)(NH2) + C2H5(OH)
а с первичными и вторичными аминами замещенные амидины. Отвечающий муравьиной кислоте этиловый формимидоэфир 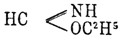 кипит при 80° и получается описанным выше способом из безводной синильной кислоты (см.). Упомянутый выше ацетимидоэфир
кипит при 80° и получается описанным выше способом из безводной синильной кислоты (см.). Упомянутый выше ацетимидоэфир  отвечает уксусной кислоте и кипит при 97°. Для этих кислот, а также для пропионовой, бензойной и др. известны, кроме этиловых, также Имидоэфиры и др. спиртов (большей частью в виде хлоргидратов). Из Имидоэфиры двухосновных кислот в свободном состоянии известны лишь отвечающие щавелевой кислоте
отвечает уксусной кислоте и кипит при 97°. Для этих кислот, а также для пропионовой, бензойной и др. известны, кроме этиловых, также Имидоэфиры и др. спиртов (большей частью в виде хлоргидратов). Из Имидоэфиры двухосновных кислот в свободном состоянии известны лишь отвечающие щавелевой кислоте  (температура плавления 25°, температура кипения 170°) и изофталевой кислоте
(температура плавления 25°, температура кипения 170°) и изофталевой кислоте  (кристаллическое вещество). Обладая характером оснований, Имидоэфиры способны образовать соединения с кислотами. Таковы упомянутые выше их хлоргидраты, представляющие прекрасно кристаллизующиеся, но малопрочные вещества. Имидоэфиры одноосновных кислот образуют хлоргидраты с одной частицей соляной кислоты, Имидоэфиры двухосновных кислот с двумя, напр. для формимидоэфира CH(OC 2H5)NH∙HCl и сукцинимидоэфира C 2H4C2(OC2H5)2(NH)2 2HCl. Хлоргидраты Имидоэфиры дают целый ряд примечательных превращений. При нагревании они распадаются на соответствующие амиды и хлорюры, напр.:
(кристаллическое вещество). Обладая характером оснований, Имидоэфиры способны образовать соединения с кислотами. Таковы упомянутые выше их хлоргидраты, представляющие прекрасно кристаллизующиеся, но малопрочные вещества. Имидоэфиры одноосновных кислот образуют хлоргидраты с одной частицей соляной кислоты, Имидоэфиры двухосновных кислот с двумя, напр. для формимидоэфира CH(OC 2H5)NH∙HCl и сукцинимидоэфира C 2H4C2(OC2H5)2(NH)2 2HCl. Хлоргидраты Имидоэфиры дают целый ряд примечательных превращений. При нагревании они распадаются на соответствующие амиды и хлорюры, напр.:
Водой и спиртами разлагаются с образованием эфиров и нашатыря:
С аммиаком дают хлоргидраты амидинов:
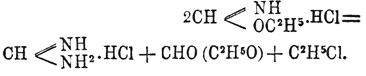
Превращения хлоргидрата формимидоэфира показывают некоторые особенности. Так, при нагревании он распадается на хлористый этил, муравьиный эфир и хлористоводородный формамидин:
Со спиртами дает ортомуравьиные эфиры:
Имидоэфиры, отвечающие угольной кислоте, также известны. Из них получены (Зандмейер, 1886) метиловый и этиловый при пропускании хлора на холоду в смесь растворов едкого натра, синеродистого калия и соответствующего спирта и затем восстановлением мышьяковистой кислотой образующихся при этом хлорзамещенных имидоугольных эфиров. Образование последних при этой сложной реакции понимается из уравнений:
С 2H5 OН + NаНО + Сl 2 = С 2H5 OСl + NaCl + Н 2O;
С 2H5 OСl + KCN = С 2H5 OCN + КСl;
C2H5OCN + C2H5OCl = (C2H5O)2CNCl.
Этиловый имидоугольный эфир (C 2H5O)2 CNH представляет растворимую в воде и сильно разлагающуюся при перегонке маслообразную жидкость с запахом триметиламина, обладает щелочной реакцией и с сухим хлористым водородом образует хлоргидрат, разлагающийся при нагревании на хлористый этил и уретан (см. Карбаминовая кислота), а при кипячении с водным аммиаком дающий гуанидин. Метиловый эфир (CH 3∙O)2 CNH представляет подобные же свойства.
П. П. Рубцов. Δ .
|
Смотрии так же... |
|