Пировиноградная кислота C3H4O3 = СН 3 —СО—СОНО (иначе: ацетилмуравьиная, метилглиоксилевая или, по новой номенклатуре, пропаноновая кислота) — простейшая α-кетонокислота (см.), открыта Берцелиусом в 1835 г., получившим ее осторожной перегонкой (не выше 220°) виноградной и винной кислот (откуда и название ее). В настоящее время она обыкновенно получается тем же путем, но с прибавкой к названным кислотам кислой серно-калиевой соли, что значительно улучшает выход продукта (Erlenmeyer). Реакция состоит здесь в отщеплении воды и углекислоты: C 4H6O6 = C3H4O3 + СО 2 + Н 2 O. Полученная кислота очищается фракционированной перегонкой, но не слишком продолжительной (см. ниже свойства). Пировиноградная кислота кислота получается также общими способами образования α-кетонокислот: из соответствующего нитрила, цианистого ацетила СН 3 —СО—CN (Claisen u. Shadwell; см. Кетонокислоты), при окислении этилиденмолочной кислоты СН 3 —СН(OН)—СОНО хамелеоном (Бейльштейн и Виганд); далее она образуется из α-дихлор- и α-дибромпропионовой кислоты при обработке их окисью серебра (Beckurts u. Otto) или действием воды при 130° (Клименко): CH 3—CBr2—CO2 H + А 2 O = СН 3 —СО—СО 2H + 2AgBr; CH3—CCl2—CO2 H + Н 2 O = CН 3 —СО—СО 2 H + 2НСl; при перегонке глицериновой кисл.: СН 2 (ОН)—СH(ОH)—СО 2 H = СН 3 —СО—СО 2 H + Н 2 O (Moldenhauer; ср. выше) и нек. др. случаях. Пировиноградная кислота кислота при обыкн. темп. жидка, на холоду застывает и вновь плавится при +9° (Simon), кипит почти без разложения при 165°, по запаху напоминает уксусную кислоту, имеет уд. в. близкий к 1,27 (20°), растворяется во всех пропорциях в воде, спирте и эфире. Как кислота (одноосновная), Пировиноградная кислота кислота образует соли, сложные эфиры и др. производные. Соли, если они получены на холоду, кристалличны; при нагревании их растворов они переходят в аморфные (полимерные?) видоизменения, как и сама кислота, которая при стоянии на холоду, быстрее при нагревании, переходит в нелетучий сироп, способный давать лишь аморфные соли. Пировиноградная кислота кислота, выделенная из нормальных солей, также является сиропообразной. Сложные эфиры Пировиноградная кислота кислоты получаются обычными путями. Метиловый эфир СН 3 —СО—СО(ОСН 3), полученный bз серебряной соли в CH 3 J, кипит при 134—137°. Этиловый эфир СН 3 —СО—СО(OC 2H5) получен при действии крепкой серной кислоты на смесь Пировиноградная кислота кислоты со спиртом, кипит при 146—146° (710 мм), водой быстро разлагается. Амид CH3—CO—CO—NH2 получен осторожной гидратацией нитрила и представляет хорошо образованные призматические или таблицеобразные кристаллы, плавящиеся при 124—125°, легко растворимые в воде и спирте и легко возгоняющиеся (ниже 100°). Нитрил Пировиноградная кислота кислоты, цианистый ацетил CH 3 —CO—CN, получается при действии синеродистого серебра на хлористый ацетил: СН 3 —СОСl + AgCN = CH 3—CO—CN + AgCl (Hü bner) или отнятием воды от изонитрозоацетона, например, при действии хлористого ацетила:
CH3—CO—CH(NOH) — H2O = CH3 —CO—CN (Claisen u. Manasse). Нитрил представляет жидкость, кипящую при 93°, под влиянием крепкой соляной кислоты превращается в Пировиноградная кислота кислоту, водой медленно разлагается на уксусную и синильную кислоты (CH 3 —CO—CN + Н 2 O = СН 3 —СОНО + HCN) и при хранении, а также при действии твердых едких щелочей, полимеризуется, образуя C 6H6O2N2. Кетонная натура Пировиноградная кислота кислоты проявляется в образовании оксима, гидразона, соединений с синильной кислотой [CH 3 —C(OH)(CN)—COHO] двусернистокислыми щелочами, аммиаком и пр., в реакциях восстановления и уплотнения. Оксим Пировиноградная кислота кислоты, или изонитрозопропионовая кислота CH 3 —C(=NO)—COHO, помимо обычного способа получения оксимов (см. Изонитрозосоединения) действием гидроксиламина (V. Meyer u. Janni), получается в виде эфира, который затем обмыливается, при действии азотистой кислоты на метилацетоуксусный эфир: CH 3—CO—CH(CH3)—CO—OC2H5 + HO—NO = CH3—C(=N—OH)CO—OC2H5 + CH3 —СООН (V. Meyer и Zublin. [Реакция, общaя для получения оксимов α-кетонокислот, исходя из однозамещенных гомологов ацетоуксусного эфира СН 3 —СО—СH(R)—СООС 2H5 (Wiengel, Fü rth).]), а также на метилмалоновый эфир: CH 3—CH(CO2H)—CO—OC2H5 + HO—NO = CH3—C(=N—OH)CO—OC2H5 + H2O +CO2; представляет белое кристаллическое вещество со свойствами кислоты, растворимое в воде, при слабом нагревании с уксусным ангидридом распадается на воду, углекислоту и ацетонитрид: CH 3—C(N—OH)—COHO = CH3—CN + CO2 + H2 O, а при нагревании до 177° сразу разлагается и исчезает без остатка. Фенилгидразон C6H5NH—N=C(CH3)—COHO образуется в виде светло-желтого объемистого кристаллического осадка (иглы, темп. плавл. 192°) при действии фенилгидразина даже на весьма слабые водные растворы Пировиноградная кислота кислоты (характерная реакция); образуется также при действии Пировиноградная кислота кислоты на др. гидразоны, например: (CH 3)2—C=N—NHC6H5 + CH3—CO—COHO = (CH3)2 —СО + CH 3—C(=N—NH—C6H5 —COHO (E. Fischer, Jourdan и Ach). При воcстановлении амальгамой натрия или цинком с соляной кислотой Пировиноградная кислота кислота дает этилиденмолочную СН 3 —СH(ОH)—СОНО (кетонная реакция, ср. Кетонокислоты); при воcстановлении йодистым водородом — пропионовую CH 3—CH2 —COHO. С др. стороны, и сама она может действовать восстановительно, выделяя серебряное зеркало из аммиачного раствора окиси серебра и окисляясь при кипячении с последней в уксусную и угольную кислоты. Из реакций уплотнения Пировиноградная кислота кислоты обращают на себя внимание идущие под влиянием оснований, напр., едкого барита (Finkh, B ö ttinger). При кипячении Пировиноградная кислота кислоты с количеством Ва(ОН) 2, недостаточным для ее нейтрализации, и в присутствии небольшого количества воды образуются рядом с уксусной и угольной кислотой кислоты пировинная CO2—CH2—CH(CH3)—CO2 H и пиротритаровая (увиновая) 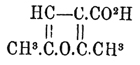 . Те же продукты и, кроме того, еще цитраконовая кислота, впрочем, получаются и просто при продолжительном нагревании Пировиноградная кислота кислоты до 170° (B ö llinger). Уплотнение с образованием пировинной кислоты происходит также при нагревании Пировиноградная кислота кислоты с соляной кислотой до 100° 2CH 3—CO—CO2 H = СО 2 H—СН 2 —СH(СН 3)—СО 2 H + СО 2 (Clermont). При кипячении Пировиноградная кислота кислоты с избытком барита образуется вместе с СО 2, C2H2O4 и др. увитиновая кислота C6H3(CO2H)2CH3 (Finkh, Bö ttinger), представляющая метилизофталевую кислоту (ср. превращение ацетона в мезитилен). В присутствии аммиака Пировиноградная кислота кислота конденсируется с образованием производных пиридина (см.). В присутствии крепкой серной кислоты на холоду Пировиноградная кислота кислота дает с углеводородами C nH2n-6 бензольного ряда кислоты С nH2n-16O2, например: CЗ H4O3 + 2C6H6 = C15H14O2 + Н 2 O. Подобным же образом она реагирует и с фенолами (B ö ttinger). Из др. реакций заслуживает упоминания действие пятихлористого фосфора РСl 5, который превращает Пировиноградная кислота кислоту в хлорангидриды моно- и дихлорпировиноградных кислот (Seissl).
. Те же продукты и, кроме того, еще цитраконовая кислота, впрочем, получаются и просто при продолжительном нагревании Пировиноградная кислота кислоты до 170° (B ö llinger). Уплотнение с образованием пировинной кислоты происходит также при нагревании Пировиноградная кислота кислоты с соляной кислотой до 100° 2CH 3—CO—CO2 H = СО 2 H—СН 2 —СH(СН 3)—СО 2 H + СО 2 (Clermont). При кипячении Пировиноградная кислота кислоты с избытком барита образуется вместе с СО 2, C2H2O4 и др. увитиновая кислота C6H3(CO2H)2CH3 (Finkh, Bö ttinger), представляющая метилизофталевую кислоту (ср. превращение ацетона в мезитилен). В присутствии аммиака Пировиноградная кислота кислота конденсируется с образованием производных пиридина (см.). В присутствии крепкой серной кислоты на холоду Пировиноградная кислота кислота дает с углеводородами C nH2n-6 бензольного ряда кислоты С nH2n-16O2, например: CЗ H4O3 + 2C6H6 = C15H14O2 + Н 2 O. Подобным же образом она реагирует и с фенолами (B ö ttinger). Из др. реакций заслуживает упоминания действие пятихлористого фосфора РСl 5, который превращает Пировиноградная кислота кислоту в хлорангидриды моно- и дихлорпировиноградных кислот (Seissl).
Пировиноградная кислота Пировиноградная кислота Рубцов. Δ .
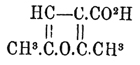 . Те же продукты и, кроме того, еще цитраконовая кислота, впрочем, получаются и просто при продолжительном нагревании Пировиноградная кислота кислоты до 170° (B ö llinger). Уплотнение с образованием пировинной кислоты происходит также при нагревании Пировиноградная кислота кислоты с соляной кислотой до 100° 2CH 3—CO—CO2 H = СО 2 H—СН 2 —СH(СН 3)—СО 2 H + СО 2 (Clermont). При кипячении Пировиноградная кислота кислоты с избытком барита образуется вместе с СО 2, C2H2O4 и др. увитиновая кислота C6H3(CO2H)2CH3 (Finkh, Bö ttinger), представляющая метилизофталевую кислоту (ср. превращение ацетона в мезитилен). В присутствии аммиака Пировиноградная кислота кислота конденсируется с образованием производных пиридина (см.). В присутствии крепкой серной кислоты на холоду Пировиноградная кислота кислота дает с углеводородами C nH2n-6 бензольного ряда кислоты С nH2n-16O2, например: CЗ H4O3 + 2C6H6 = C15H14O2 + Н 2 O. Подобным же образом она реагирует и с фенолами (B ö ttinger). Из др. реакций заслуживает упоминания действие пятихлористого фосфора РСl 5, который превращает Пировиноградная кислота кислоту в хлорангидриды моно- и дихлорпировиноградных кислот (Seissl).
. Те же продукты и, кроме того, еще цитраконовая кислота, впрочем, получаются и просто при продолжительном нагревании Пировиноградная кислота кислоты до 170° (B ö llinger). Уплотнение с образованием пировинной кислоты происходит также при нагревании Пировиноградная кислота кислоты с соляной кислотой до 100° 2CH 3—CO—CO2 H = СО 2 H—СН 2 —СH(СН 3)—СО 2 H + СО 2 (Clermont). При кипячении Пировиноградная кислота кислоты с избытком барита образуется вместе с СО 2, C2H2O4 и др. увитиновая кислота C6H3(CO2H)2CH3 (Finkh, Bö ttinger), представляющая метилизофталевую кислоту (ср. превращение ацетона в мезитилен). В присутствии аммиака Пировиноградная кислота кислота конденсируется с образованием производных пиридина (см.). В присутствии крепкой серной кислоты на холоду Пировиноградная кислота кислота дает с углеводородами C nH2n-6 бензольного ряда кислоты С nH2n-16O2, например: CЗ H4O3 + 2C6H6 = C15H14O2 + Н 2 O. Подобным же образом она реагирует и с фенолами (B ö ttinger). Из др. реакций заслуживает упоминания действие пятихлористого фосфора РСl 5, который превращает Пировиноградная кислота кислоту в хлорангидриды моно- и дихлорпировиноградных кислот (Seissl).