Кротоновая кислота
Энциклопедия Брокгауза Ф.А. и Ефрона И.А. (1890 - 1916гг.) Статьи для написания рефератов, курсовых работ, научные статьи, биографии (118447 статей и 6000 рисунков).
|
|
| А | Б | В | Г | Д | Е | Ё | Ж | З | И | Й | К | Л | М | Н | О | П | Р | С | Т | У | Ф | Х | Ц | Ч | Ш | Щ | Ы | Э | Ю | Я | A | B | C | D | E | F | G | H | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | Z |
| К | КЫ | КА | КВ | КГ | КЕ | КЁ | КИ | КЛ | КМ | КН | КО | КР | КС | КТ | КУ | КХ | КШ | КЫ | КЬ | КЭ | КЮ | КЯ |
| КРА |
| КРЕ |
| КРЖ |
| КРИ |
| КРЛ |
| КРО |
| КРС |
| КРУ |
| КРШ |
| КРЫ |
| КРЭ |
| КРЮ |
| КРЯ |
Кротоновая кислота (xим.) С 4 Н 6O2 =СН 3 -СН=СН-COOH — получила свое название от растения Croton tiglium, из масла которого была выделена непредельная кислота, отвечавшая по составу написанной формуле. Впоследствии оказалось, что состав этой кислоты гораздо сложнее и что собственно Кротоновая кислота кислоты в Кротоновая кислота масле нет, но усвоенное этой кислоте название осталось и даже другие две изомерные кислоты состава С 4 Н 6O2 называются Кротоновая кислота Обыкновенная твердая Кротоновая кислота кисл. кристаллизуется при охлаждении горячего водного раствора в виде тонких иголок с темп. пл. 71-72°, кипит пpи 180-181°. Получается она восстановлением ацетоуксусного эфира амальгамой натрия в присутствии воды: CH 3.CO.CH2.CO2.C2H5+2H=CH3.CH(OH).CH2.CO2.C2H5 и затем перегонкой продуктов реакции, подкисленных серной кислотой, с водяным паром. При этом отщепляется от образовавшейся β-оксимасляной кислоты вода и Кротоновая кислота кисл. перегоняется с парами воды. Соли кальция (С 4 Н 5O2)2 Ca и бария (С 4 Н 5O2)2 Ba кристаллизуются безводными и в воде хорошо растворимы. Этиловый эфир С 4 Н 5O2.C2 Н 5 кипит при 139,5-141,5°. Непредельность Кротоновая кислота кисл. определяется способностью ее присоединять два атома хлора или брома. Строение Кротоновая кислота кисл. СН 3 -СН=СН-СООН доказывается образованием ее: 1) из α-бромомасляного эфира при действии спиртовой щелочи; 2) из кротонового альдегида при окислении. Продукты распадения Кротоновая кислота кислоты при окислении — уксусный альдегид и щавелевая кислота — также подтверждают данное строение. Кажущийся противоречием подобному воззрению на вышеуказанное строение факт образования ее из так назыв. цианистого аллила устраняется тем, что цианистый аллил имеет строение, не соответствующее его названию. Другой изомер твердой Кротоновая кислота кисл. имеет также четыре атома углерода, цепеобразно-связанных, так как присоединением частицы бромистого или йодистого водорода и затем восстановлением она превращается в нормальную масляную кислоту. Эта изомерная кислота носит название изокротоновой (β-кротоновой, квартениловой кисл.). Она представляет жидкость с запахом, напоминающим масляную кислоту, не застывающую при -15°, кипящую при 172°, с водой во всех отношениях смешивающуюся. Соли кальция и бария в воде легкорастворимы и кристаллизуются обе с двумя частицами воды; этиловый эфир ее кипит при 136°. При действии пятихлористого фосфора на ацетоуксусный эфир получаются две изомерных кислоты состава С 4 Н 5 СlO 2, частью в виде их этиловых эфиров, частью же в виде хлоропродуктов:
СН 3.СО.СН 2.СО 2.C2H5 + РС1 5 = СН 3.ССl 2.СН 2.СО 2.С 2H5 + POCl3;
2CH3.CCl2.CH2.CO2.C2H5 -2НСl = СН 3.ССl: СH.СО 2.С 2H5 + СН 2:ССlСН 2.СО 2.С 2H5.
Хлоропродукты разделяются перегонкой с водяным паром, причем перегоняется только первый, который при восстановлении амальгамой натрия дает твердую Кротоновая кислота кисл., чем в подтверждается вышеуказанное его строение. Второй хлоропродукт, не перегоняющийся с водяным паром, при восстановлении дает изокротоновую кислоту. Так как данное строение второго хлоропродукта гипотетично, то и строение самой изокротоновой кислоты этим способом получения еще не определяется. С точки зрения структурной теории для непредельной кислоты состава C 4H6O2, имеющей углеродные атомы цепеобразно-связанные, может быть только два изомера: 1) СН 3.CH:СН.СООН и 2) СН 2:CH.CH2.COOH, и, стало быть, строго держась только этой теории, нужно признать, что изокротоновая кислота имеет второе строение, так как первое несомненно принадлежит твердой Кротоновая кислота кисл. Но с точки зрения теории пространственного расположения атомов, твердая Кротоновая кислота кисл., представляя по своему строению симметрично двузамещенный этилен, может иметь геометрический изомер с тем же строением. Этот вопрос, структурный ли или геометрический изомер изокротоновая кислота по отношению к твердой Кротоновая кислота, еще не выяснен окончательно. Скорее можно признать последнее. В пользу такого представления говорит легкая способность перехода при нагревании до 170-180° изокротоновой кислоты в Кротоновая кислота и полнейшее тождество превращений этих кислот с превращениями геометрических изомеров коричной кислоты, имеющей сходное строение: СН 3.СН : СН.СООН (Кротоновая кислота кислота), C 6H5.СН:СН.СОOН (коричная кислота). Принимая Кротоновая кислота и изокротоновую кислоты за геометрические изомеры, нужно признать, что твердая Кротоновая кислота кисл. имеет следующую конфигурацию: (cis) 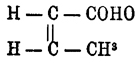 , так как при восстановлении тетроловой кислоты получается твердая Кротоновая кислота кислота:
, так как при восстановлении тетроловой кислоты получается твердая Кротоновая кислота кислота:
СН 3 — С ≡ С — СООН + Н 2 = СН 3 — СН = СН — СООН.
Тогда изокротоновая кислота будет иметь такую конфигурацию: (cis-trans) 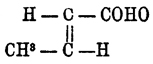 . Вопрос об изомерии Кротоновая кислота кислот будет окончательно решен, если будет получена кислота строения СН 2 =СН-СН 2 -СООН, которая до сих пор еще неизвестна. Обе Кротоновая кислота кисл. встречаются в продуктах сухой перегонки дерева. К числу структурных изомеров Кротоновая кислота кисл. принадлежит метакриловая кислота или α-метилакриловая СН 2: C(CH3).COOH. Получается она действием трехлористого фосфора на оксиизомасляную кислоту:
. Вопрос об изомерии Кротоновая кислота кислот будет окончательно решен, если будет получена кислота строения СН 2 =СН-СН 2 -СООН, которая до сих пор еще неизвестна. Обе Кротоновая кислота кисл. встречаются в продуктах сухой перегонки дерева. К числу структурных изомеров Кротоновая кислота кисл. принадлежит метакриловая кислота или α-метилакриловая СН 2: C(CH3).COOH. Получается она действием трехлористого фосфора на оксиизомасляную кислоту:
3(СН 3)2 C(ОН)CООН + РС l3 = 3СН 2:С(CН 3).СОНО + РН 3O3 + 3НС l.
Метакриловая кислота образуется также из α-бромоизомасляной кислоты:
(СH 3)2 CBr.СОНО — HBr = CH 2: C(CH3)COHO.
Эти способы получения вполне устанавливают строение метакриловой кислоты. Кристаллизуется она из воды при охлаждении в бесцветных длинных призмах, плавится при 16°, кипит при 160-161°, имеет довольно сильный и приятный запах, растворяется в теплой воде, спирте и эфире во всех пропорциях. Кальциевая соль ее кристаллизуется в длинных, тонких иголках. Метакриловая кислота легко восстановляется водородом в изомасляную кислоту; присоединяет галоидоводородные кислоты, образуя β-галоидопроизводные, например:
СН 2: С(CН 3).СООН + HBr = СН 2Br.CH(CH3).СООН;
при нагревании или в соприкосновении с соляной кислотой при обыкновенной температуре она полимеризуется в аморфную, белую массу, нерастворимую в воде и обладающую свойствами слабой кислоты.
Кротоновая кислота Kpacycкuй. Δ.
|
Смотрии так же... |
|