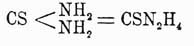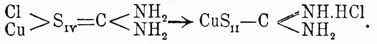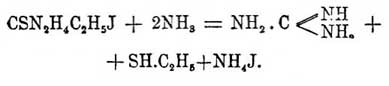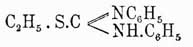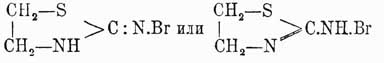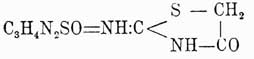Тиомочевины
Энциклопедия Брокгауза Ф.А. и Ефрона И.А. (1890 - 1916гг.) Статьи для написания рефератов, курсовых работ, научные статьи, биографии (118447 статей и 6000 рисунков).
|
|
| А | Б | В | Г | Д | Е | Ё | Ж | З | И | Й | К | Л | М | Н | О | П | Р | С | Т | У | Ф | Х | Ц | Ч | Ш | Щ | Ы | Э | Ю | Я | A | B | C | D | E | F | G | H | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | Z |
| Т | ТА | ТВ | ТЕ | ТЁ | ТЗ | ТИ | ТК | ТЛ | ТМ | ТО | ТР | ТС | ТУ | ТХ | ТЦ | ТШ | ТЩ | ТЫ | ТЬ | ТЭ | ТЮ | ТЯ |
| ТИА |
| ТИБ |
| ТИВ |
| ТИГ |
| ТИД |
| ТИЕ |
| ТИЗ |
| ТИИ |
| ТИК |
| ТИЛ |
| ТИМ |
| ТИН |
| ТИО |
| ТИП |
| ТИР |
| ТИС |
| ТИТ |
| ТИУ |
| ТИФ |
| ТИХ |
| ТИЦ |
| ТИЧ |
| ТИШ |
| ТИЩ |
| ТИЯ |
Тиомочевины (химич.), тиокарбамиды. Исходным веществом для всех относящихся сюда соединений служит Тиомочевины, или тиокарбамид
амид тиоугольной кислоты (см.), или мочевина (см.), в которой кислород замещен серой. Полная аналогия Тиомочевины с мочевиной, основанная на общих реакциях образования этих тел, служит доказательством ее строения, выражаемого приведенной выше формулой. Известно, однако, что многие Тиомочевины не отвечают этой формуле, а являются производными таутомерной формы, так наз. имидотиокарбаминовой кислоты (Bemthsen) или меркаптана, отвечающего формамидину (Курнаков), т. е. 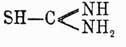 , изо-Тиомочевины, под влиянием различных внешних условий образующейся лишь в момент некоторых реакций и не существующей в свободном состоянии. Впрочем, образование изо-Тиомочевины можно объяснить и иначе, не прибегая к таутомерным формам (Claus). T. получается путем след. реакций. 1) Изомеризацией роданистого аммония при нагревании до температуры плавления (Рейнольдс): CN—S—NH4 = NH2—CS—NH2. Когда начинается выделение сероводорода, аммиака и паров сернистого углерода, смесь быстро охлаждают и обрабатывают безводным спиртом для извлечения вновь образующегося из Тиомочевины роданистого аммония, потом кристаллизуют из горячей воды. Эта реакция вполне аналогична синтезу мочевины, но как там, так и здесь самый механизм внутримолекулярной перегруппировки остается пока темным. 2) Присоединением элементов сероводорода к цианамиду при продолжительном действии избытка желтого сернистого аммония на насыщенный водный раствор цианамида или же при пропускании сухого сероводорода в эфирный раствор этого соединения (Baumann): CN—NH 2 + H2S = NH2—CS—NH2. 3) Действием на цианамид тиоуксусной кислоты (Baumann, Praetorius-Seidler). 4) Восстановлением изоперсульфоциановой кислоты йодистым водородом или оловом и соляной кислотой (Glutz). 5) Действием аммиака на сероокись углерода, при чем образуется также и мочевина (Berthelot). Из горячего водного раствора, содержащего роданистый аммоний, Тиомочевины кристаллизуется в длинных, белых, с перламутровым блеском иглах. Чистая Тиомочевины образует толстые ромбические кристаллы, плавящиеся при 180° (Hantzsch), уд. в. = 1,406 (в бензоле) и 1,450 (в оливковом масле; Schr ö der); горька на вкус, растворяется в 11 ч. холодной воды, почти нерастворима в спирте и эфире; по Армстронгу, имеет удвоенную молекулу C 2S2N4H8. T. легко переводится обратно в роданистый аммоний и в цианамид. Обратная перегруппировка в CNSNH 4 замечается уже при 160—170°; тот же процесс имеет место при нагревании с водой в зап. трубке при 140° и на холоду при действии спиртового раствора азотисто-этилового эфира. Последнюю реакцию Клаус предлагает для открытия Тиомочевины: если Тиомочевины находится в исследуемой смеси, то при прибавлении азотистого эфира и хлорного железа образующийся из нее роданистый аммоний дает красное окрашивание. Сама Тиомочевины окрашивания с хлорным железом не дает. Переход в цианамид наблюдается при действии свежеосажденной окиси ртути на холоду:
, изо-Тиомочевины, под влиянием различных внешних условий образующейся лишь в момент некоторых реакций и не существующей в свободном состоянии. Впрочем, образование изо-Тиомочевины можно объяснить и иначе, не прибегая к таутомерным формам (Claus). T. получается путем след. реакций. 1) Изомеризацией роданистого аммония при нагревании до температуры плавления (Рейнольдс): CN—S—NH4 = NH2—CS—NH2. Когда начинается выделение сероводорода, аммиака и паров сернистого углерода, смесь быстро охлаждают и обрабатывают безводным спиртом для извлечения вновь образующегося из Тиомочевины роданистого аммония, потом кристаллизуют из горячей воды. Эта реакция вполне аналогична синтезу мочевины, но как там, так и здесь самый механизм внутримолекулярной перегруппировки остается пока темным. 2) Присоединением элементов сероводорода к цианамиду при продолжительном действии избытка желтого сернистого аммония на насыщенный водный раствор цианамида или же при пропускании сухого сероводорода в эфирный раствор этого соединения (Baumann): CN—NH 2 + H2S = NH2—CS—NH2. 3) Действием на цианамид тиоуксусной кислоты (Baumann, Praetorius-Seidler). 4) Восстановлением изоперсульфоциановой кислоты йодистым водородом или оловом и соляной кислотой (Glutz). 5) Действием аммиака на сероокись углерода, при чем образуется также и мочевина (Berthelot). Из горячего водного раствора, содержащего роданистый аммоний, Тиомочевины кристаллизуется в длинных, белых, с перламутровым блеском иглах. Чистая Тиомочевины образует толстые ромбические кристаллы, плавящиеся при 180° (Hantzsch), уд. в. = 1,406 (в бензоле) и 1,450 (в оливковом масле; Schr ö der); горька на вкус, растворяется в 11 ч. холодной воды, почти нерастворима в спирте и эфире; по Армстронгу, имеет удвоенную молекулу C 2S2N4H8. T. легко переводится обратно в роданистый аммоний и в цианамид. Обратная перегруппировка в CNSNH 4 замечается уже при 160—170°; тот же процесс имеет место при нагревании с водой в зап. трубке при 140° и на холоду при действии спиртового раствора азотисто-этилового эфира. Последнюю реакцию Клаус предлагает для открытия Тиомочевины: если Тиомочевины находится в исследуемой смеси, то при прибавлении азотистого эфира и хлорного железа образующийся из нее роданистый аммоний дает красное окрашивание. Сама Тиомочевины окрашивания с хлорным железом не дает. Переход в цианамид наблюдается при действии свежеосажденной окиси ртути на холоду:
NH2—CS—NH2 + HgO = NH2—CN + HgS + H2O
при 100° образуется дициандиамид (Hofmann, Baumann, Volhard). Окись ртути можно заменить сулемой, приливая потом щелочи: NH 2—CS—NH2 + HgCl2 + 2KOH = NH2—CN + HgS + 2KCl + 2H2 O; подобным же образом действует и окись свинца. Реакции окисления протекают различно: при окислении раствором марганцовокислого калия в нейтральной среде (Maly) образуется мочевина; наоборот, при действии марганцовокислого калия в кислом растворе, а также йода, перекиси водорода и двухромовокалиевой соли — образуется дитиопродукт строения:
Щелочи разлагают Тиомочевины; полное разложение наступает при нагревании в зап. трубке с раствором едкого кали до 100°, при чем образуются углекислота, аммиак, сероводород и роданистый калий. При нагревании Тиомочевины до 170—180° образуются роданистый гуанидин и тиоуглекислый аммоний:
5CSN2H4 = 2CH5N3CHSN + (NH4)2CS3.
Для Тиомочевины в высшей степени характерна способность к самым разнообразным реакциям присоединения, обусловленная присутствием в ее частице атома серы. Она легко соединяется с галоидами, кислотами, некоторыми металлическими окисями, солями многих металлов и с целым рядом органических веществ. Соединения с хлором, бромом и йодом имеют состав (CSN 2H4)2X2 (Claus, Macgowan); из соединений с кислотами наиболее характерно CSN 2H4·HNO3. Сочетания Тиомочевины с различными солями свинца, кадмия, ртути, олова, висмута, серебра, таллия, меди, платины и палладия исследовали Рейнольдс, Клаус, Мали, Преториус-3ейдлер, Ратке, Курнаков и др. Состав всех этих двойных солей отвечает общей формуле nCSN 2H4·MXm, где M — металл, а X — кислотный остаток. В известных до настоящего времени солях коэффициент n изменяется в пределах от 3 до 4 (на 1 атом металла). При взаимодействии с солями окиси меди Тиомочевины реагирует сначала как восстановитель, причем образующаяся соль закиси вступает затем в сочетание с новым количеством Тиомочевины (Rathke). Высшее платиновое соединение имеет состав (CSN 2H4)4PtCl2 (Курнаков). Эти соли отличаются значительным постоянством в присутствии кислот и не разлагаются сероводородом. Вообще говоря, наиболее прочные сочетания Тиомочевины образует с солями металлов, которые осаждаются сернистым водородом из кислых растворов или, говоря другими словами, дают более стойкие, не разлагаемые кислотами сернистые соединения. С другой стороны, при замещении серы в Тиомочевины другими группами получаются вещества, в которых способность к соединению или ослаблена, или даже совсем уничтожена. Далее, нужно заметить, что Тиомочевины в соединениях с кислотами и солями является однокислотным основанием, между тем как содержит две амидогруппы. Наконец, изучение реакции галоидалкилов на Тиомочевины (см. ниже) показывает, что действие присоединяющихся веществ направляется прежде всего на серу. На основании всех этих соображений полагают, что сера Тиомочевины принимает непосредственное участие в акте сочетания, причем образуются производные изо-Тиомочевины, строение которых, напр. для солей меди, будет такое:
 (Rathke. См. Курнаков, "Ж. Р. х. общ.", 25, 565 и сл.).
(Rathke. См. Курнаков, "Ж. Р. х. общ.", 25, 565 и сл.).
Исходя из симметрической формулы Тиомочевины, образование таких соединений можно объяснить следующей схемой:
Продукты присоединения галоидалкилов открыты Клаусом. Так, напр., при действии йодистого метила на Тиомочевины образуется твердое кристаллическое вещество с темп. пл. 317°, легко растворимое в воде и спирте и выделяющее при обработке окисью серебра свободное основание, которое сообщает раствору сильнощелочную реакцию. Эти соединения способны разлагаться с выделением тиоспиртов. Напр., продукт присоединения йодистого этила к Тиомочевины при кипячении с раствором аммиака распадается на гуанидин и меркаптан:
Эта реакция показывает, что углеводородный остаток здесь связан непосредственно с серой, на основании чего такого рода соединениям придают состав 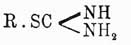 , считая их производными изо-Тиомочевины (Bernthsen u. Klinger, Will, Rathke и др.). Кроме галоидов, кислот и металлических солей, Тиомочевины вступает в сочетание еще со мн. др. веществами: с бромистым кремнием образуются соединения 8CSN 2H4—SiBr4 и др., хлористый ацетил дает CSN 2H4—C2H3 OCl, щавелево-этиловый эфир образует 2CSN 2H4—C2 О 4 (С 2 Н 5)2; описаны соединения с альдегидами (причем выделяется вода), альдегидаммиаком, хлоралгидратом, аминами и мн. др. Замещенные Тиомочевины получены в очень большом числе. Водород амидных групп может замещаться как углеводородными, так и кислотными радикалами, причем в том и другом случае получаются аналоги замещенных мочевин. Общий способ образования алкилозамещенных Тиомочевины состоит в действии аммиака и аминов на горчичные масла (Hofmann):
, считая их производными изо-Тиомочевины (Bernthsen u. Klinger, Will, Rathke и др.). Кроме галоидов, кислот и металлических солей, Тиомочевины вступает в сочетание еще со мн. др. веществами: с бромистым кремнием образуются соединения 8CSN 2H4—SiBr4 и др., хлористый ацетил дает CSN 2H4—C2H3 OCl, щавелево-этиловый эфир образует 2CSN 2H4—C2 О 4 (С 2 Н 5)2; описаны соединения с альдегидами (причем выделяется вода), альдегидаммиаком, хлоралгидратом, аминами и мн. др. Замещенные Тиомочевины получены в очень большом числе. Водород амидных групп может замещаться как углеводородными, так и кислотными радикалами, причем в том и другом случае получаются аналоги замещенных мочевин. Общий способ образования алкилозамещенных Тиомочевины состоит в действии аммиака и аминов на горчичные масла (Hofmann):
C2H5—N=CS + NH3 = C2H5—NH—CS—NH2
C2H5—N=CS + C2H5NH2 = C2H5—NH—CS—NH—C2H5.
Со вторичными аминами образуются трехзамещенные Тиомочевины Несимметрические двузамещенные Тиомочевины получаются при действии сероводорода и аммиака на спиртовой раствор двузамещенных цианамидов (Wallach), напр.:
CN—N(CH3)2 + H2 S = NН 2 СS—N(СН 3)2
а также при изомеризации родановых солей вторичных аминов. Последняя реакция с жирными аминами почти не удается (Salkowsky). Тетраэтил-Тиомочевины образуется при нагревании триэтил-Тиомочевины с йодистым этилом (Grodzski). Подобные же весьма многочисленные реакции ведут к образованию замещенных Тиомочевины с ароматическими углеводородными остатками. Замещенные изо-Тиомочевины тоже известны. Сюда прежде всего относятся описанные выше продукты присоединения галоидалкилов к Тиомочевины Таким же путем из замещенных Тиомочевины были получены и другие замещенные изо-Тиомочевины, напр.
этилдифенилизо-Тиомочевины:
Циклические изомеры замещенных Тиомочевины называются псевдо-Тиомочевины Они были получены Габриелем частью при действии бромистого этиламина и его гомологов на горчичные масла или роданистый калий, частью при нагревании замещенных Тиомочевины с непредельными радикалами с крепкой соляной кислотой в запаянной трубке при 100°. Образующиеся при этих реакциях вещества являются производными тиазолина и в простейшем случае имеют строение, выражаемое одною из следующих формул:
что доказывается реакциями их окисления. Псевдоэтилен-Тиомочевины в свободном состоянии представляет жидкость, легко растворимую в йоде; она сильно изменяет лакмус и легко титруется. Вступление углеводородных остатков в частицу Тиомочевины увеличивает ее способность к реакциям присоединения. Замещенные Тиомочевины точно так же соединяются с кислотами, металлическими солями и пр., образуют замещенные цианамиды при действии окиси ртути, если в их частице сохранилась первичная амидная группа; в противном случае образуются замещенные мочевины. Последние также образуются при действии окиси свинца на все однозамещенные Тиомочевины; трехзамещенные и, по всей вероятности, четырехзамещенные Тиомочевины остаются без изменения; двузамещенные Тиомочевины теряют серу лишь тогда, когда один или оба заместителя принадлежат к ароматическому ряду (Dixon). При замещении кислотными радикалами атомов водорода Тиомочевины образуются соответствующие тиоуреиды. Ацетил-Тиомочевины получается при действии уксусного ангидрида на Тиомочевины согласно равенству:
CS(NH2)2 + (CH3CO)2O = CH3—CO—NH—CS—NH2 + CH3—COOH (Ne nzki). Она образует призматические кристаллы с темп. плавл. 165°. Тиогидантоин
получается при действии хлороуксусной кислоты на Тиомочевины: CH 2Cl—COOH + (NH2)CS = C3H4N2 SO—HCl и представляет производное изо-Тиомочевины, так как при кипячении с баритовой водой он выделяет тиогликолевую кисл. СН 2 (SH)—СООН (Liebermann u. Lange). Исследования Андреаша показали, что одно- и двузамещенные Тиомочевины соединяются с цианом; этим путем были получены производные тиопарабановой кислоты (см. Тиохолестрофан).
Д. Монастырский. Δ .
|
Смотрии так же... |
|