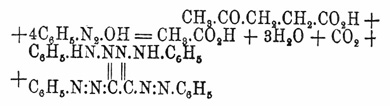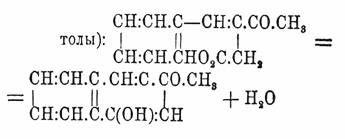Левулиновая кислота
Энциклопедия Брокгауза Ф.А. и Ефрона И.А. (1890 - 1916гг.) Статьи для написания рефератов, курсовых работ, научные статьи, биографии (118447 статей и 6000 рисунков).
|
|
| А | Б | В | Г | Д | Е | Ё | Ж | З | И | Й | К | Л | М | Н | О | П | Р | С | Т | У | Ф | Х | Ц | Ч | Ш | Щ | Ы | Э | Ю | Я | A | B | C | D | E | F | G | H | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | Z |
| ЛА | ЛБ | ЛЕ | ЛЖ | ЛИ | ЛЛ | ЛО | ЛУ | ЛХ | ЛЫ | ЛЬ | ЛЭ | ЛЮ | ЛЯ |
| ЛЕА |
| ЛЕБ |
| ЛЕВ |
| ЛЕГ |
| ЛЕД |
| ЛЕЕ |
| ЛЕЖ |
| ЛЕЗ |
| ЛЕЙ |
| ЛЕК |
| ЛЕЛ |
| ЛЕМ |
| ЛЕН |
| ЛЕО |
| ЛЕП |
| ЛЕР |
| ЛЕС |
| ЛЕТ |
| ЛЕУ |
| ЛЕФ |
| ЛЕХ |
| ЛЕЦ |
| ЛЕЧ |
| ЛЕШ |
| ЛЕЩ |
| ЛЕЭ |
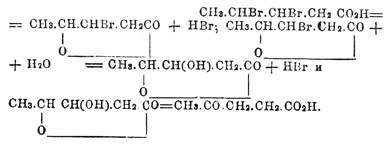
Левулиновая кислота (хим.) С 5 Н 8 О 3 =СН 3.СО 2 СН 2.СН 2.СО 2 Н или β-ацетилпропионовая (4-пентаноновая, ср. Номенклатура химическая) — является первой возможной предельной γ-кетонокислотой (см.). Ее кальциевая соль была получена еще в 1840 г. Мульдером при насыщении известью продуктов реакции разбавленных кислот на сахар. Нёльдеке, Толленс с учениками, Конрад и Вольф установили вышеприведенное строение (см. ниже). Толленс показал, что Левулиновая кислота кисл. является характерным продуктом для гексоз при реакции их с кислотами (особенно легко она образуется из d-фруктозы-левюлозы, откуда и происходит название Левулиновая кислота кислота; см. Гидраты углерода и Глюкозы. Для получения. Левулиновая кислота кислоты нагревают 20 часов на водяной бане раствор 3 кг. картофельного крахмала в 3 литр. соляной кислоты (уд. в. 1,1), отфильтровывают и отжимают образующиеся одновременно гуминовые вещества (см.) и отгоняют под уменьшенным давлением сначала воду, соляную и муравьиную кислоты, а затем и Левулиновая кислота кислоту (выход около 390 гр., т. е. около 1/5 теории; Ришбит [Предполагая, что реакция идет по уравнению: С 6 Н 12 О 6 =С 5 Н 8 О 3 +Н 2 O+СН 2O2 (муравьиная кислота)]). Синтетически Левулиновая кислота кислота получена действием хлороуксусного эфира на натрацетоуксусный эфир (см.) и из продукта присоединения брома к аллилуксусной кислоте (см. Кетонокислоты) [Данные в ст. Кетонокислоты уравнения должны быть исправлены следующим образом:
Чистая Левулиновая кислота кислота кристаллизуется в больших, блестящих кристаллах (Эрдман); плавится при 33,5°, кипит под обыкновенным давлением с разложением (см. ниже) около 250°; легко растворяется в воде. При восстановлении Левулиновая кислота кислоты переходит в γ-оксивалериановую кислоту C 5H8O3+H2= СН 3.СН(ОН).СН 2.СН 2.СО 2 Н (Вольф) и, окончательно, в нормальную валериановую кислоту: С 5H8O3 +2Н 2 -Н 2 О=СН 3.[СH 2]3.СО 2 Н (Керер и Толленс). Как кетонокислота Левулиновая кислота кислота peaгирует с HCN, образуя мононитрил α -оксиметилглутаровой кислоты CH3.CO.CH2.CH2.CO2 H+НСN=СН 3.С[(ОН)(СN)].СН 2.СН 2.СО 2 H, с гидроксиламином, с фенилгидразином и т. д. При действии едкой щелочи и йода она образует йодоформ (Толленс; см. Йодоформ), а едкой щелочи и брома — четырехбромистый углерод (Валлах; обе реакции характерны длявеществ, содержащих в частице, группу СН 3.СО', или могущих ее давать). При продолжительном нагревании под обыкновенным давлением Левулиновая кислота кислота разлагается, выделяя воду и образуя смесь двух изомерных ангеликалактонов: C5H8O3-H2O=C5H6O2 (Вольф). С диазобензолом (см.) Левулиновая кислота кисл. образует диформазил:
С альдегидами Левулиновая кислота кислота легко уплотняется, давая разнообразные продукты, из которых наиболее замечательна β - бензальлевулиновая кислота (γ - фенил-β -ацетоизокротоновая кислота), образующаяся при уплотнении (в кислом растворе) Левулиновая кислота кисл. с бензойным альдегидом: С 5 Н 8 О 3 + С 6 Н 5.СОН = СН 3.СО.С:(СН.С 6 Н 5).СН 2 СО 2 Н, дающая при перегонке 3-ацето-1-нафтол (см. Нафтолы):
Известны еще многочисленные производные как самой, так и замещенных (хлоро-, бромо— и т. д.) Левулиновая кислота кислот.
А. И. Горбов. Δ.
|
Смотрии так же... |
|