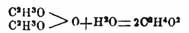Гидратация
Энциклопедия Брокгауза Ф.А. и Ефрона И.А. (1890 - 1916гг.) Статьи для написания рефератов, курсовых работ, научные статьи, биографии (118447 статей и 6000 рисунков).
|
|
| А | Б | В | Г | Д | Е | Ё | Ж | З | И | Й | К | Л | М | Н | О | П | Р | С | Т | У | Ф | Х | Ц | Ч | Ш | Щ | Ы | Э | Ю | Я | A | B | C | D | E | F | G | H | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | Z |
| Г | ГА | ГВ | ГД | ГЕ | ГЖ | ГЗ | ГИ | ГЛ | ГМ | ГН | ГО | ГР | ГУ | ГФ | ГХ | ГЫ | ГЬ | ГЭ | ГЮ | ГЯ |
| ГИА |
| ГИБ |
| ГИВ |
| ГИГ |
| ГИД |
| ГИЕ |
| ГИЖ |
| ГИЗ |
| ГИК |
| ГИЛ |
| ГИМ |
| ГИН |
| ГИО |
| ГИП |
| ГИР |
| ГИС |
| ГИТ |
| ГИУ |
| ГИФ |
| ГИХ |
| ГИЦ |
| ГИЧ |
| ГИШ |
| ГИЭ |
| ГИЯ |
Гидратация — общее название, прилагаемое обыкновенно ко всем тем химическим реакциям, при которых происходит присоединение воды. Реакции эти чрезвычайно многочисленны и разнообразны, совершаются повсюду в природе и беспрестанно применяются как в лабораторной практике, так и в различных производствах. При всем их разнообразии можно ясно различить три типа реакций Гидратация: 1) прямые реакции соединения с водой; 2) реакции соединения, совершающиеся при участии хим. деятелей, и 3) гидролиз или разложения (образование двух или более веществ из одного + вода), производимые водой через ее присоединение, большей частью также требующие воздействия третьего тела.
Прямо соединяются с водой: кислотные и основные (щелочные и щелочноземельные) ангидриды, образуя соответствующие гидраты; безводные соли, а также многие из вышеупомянутых гидратов, образуя кристаллогидраты; простые эфиры многоатомных спиртов, образуя соответствующие спирты. Все эти реакции за немногими исключениями (напр. переход метафосфорной кислоты в ортофосфорную, Гидратация окиси этилена и некотор. др.) идут более или менее легко и быстро либо при простом соприкосновении с водой, либо при растворении в ней, и сопровождаются отделением тепла, часто весьма значительным [Некоторые случаи Гидратация ангидридов соединены с распадением сложной частицы на 2 простейшие, напр. уксусный анг., соединяясь с водой, распадается с образованием 2 частиц уксусной кислоты:
Тем не менее, эта и др., подобные ей, реакции по всему своему характеру принадлежат к 1-ой группе реакций Гидратация точно так же, как образование хлористого водорода из хлора и водорода (Н 2 + Cl2 = 2НCl) есть реакция соединения. Реакции разложения водой хлорангидридов кислот, в сущности, представляют также реакции Гидратация, сходные с Гидратация смешанных кислотных ангидридов.]. Вторая группа реакций Гидратация обнимает собой сравнительно немногие случаи присоединения воды к непредельным соединениям, как то: Гидратация этиленных углеводородов в одноатомные предельные спирты и непредельных одноатомных спиртов в гликоли при нагревании их с разведенными кислотами, присоединение воды к ацетилену, пропаргиловому спирту и т. п. в присутствии бромной ртути и Гидратация некоторых терпенов под влиянием кислот. Несравненно более разнообразны реакции гидролиза. Сюда относятся: омыление (см.) сложных эфиров водой и основаниями, при чем происходит распадение эфиров на спирт и кислоту
C2H3 O.С 2H5 O (уксусноэтиловый эфир) + Н 2O = C2H4O2 (уксусн. эт. спирт) + C 2H6O;
гидролиз при кипячении с разведенными кислотами или под влиянием неорганизованных ферментов (диастаза, растворимого фермента дрожжей и друг.), глюкозидов [напр.:
С 13 Н 18 О 7 (салицин) + Н 2O = C6 Н 12O6 (глюкоза) + C7H8O2 (салигенин)]
и углеводов (напр. превращение крахмала при действии диастаза солода в мальтозу:
(C6H10O5)n + (Н 2O)n = nC6H12O6,
и инверсия сахара
(C12H22O11 (сахар) + H 2O = C6H12O6 (глюкоза) + C 6H12O6 (фруктоза);
Гидратация нитрилов, илидов, амидов и аминовых кислот, распадающихся при действии водных минеральных кислот или оснований на кислоты и аммиак (напр.
С 2O2(NH2)2 (оксамид) + 2Н 2O = C2H2O4 (щавел. к.) + 2NH 3 или CNOH (циановая кисл.) + Н 2 O = СО 2 (углек.) + NH 3;
Гидратация с помощью кислот альдоксимов, кетоксимов и гидроксамовых кислот, гидразонов и озазонов, которые разлагаются при этом на альдегиды, кетоны, кислоты, глюкозы и оксиглюкозы, с одной стороны, и гидроксиламин и фенилгидразин, с другой, и, наконец, реакции Гидратация амидоксимов, изонитрилов, ортоэфиров, имидоэфиров, ангидримидокислот и амидинов и некотор. др. Более сложные относящиеся сюда случаи Гидратация представляют белковые вещества. Таковы процессы пептонизации белков (см. Пептоны) под влиянием, напр., неорганизованного фермента желудочного сока, пепсина, в присутствии слабой соляной кислоты и процессы гниения их [Здесь Гидратация соединена с окислением.] под влиянием жизнедеятельности особых бактерий, сопровождающиеся постепенным распадом белковых тел с образованием сперва пептонов, лейцина и тирозина и далее аммиака, сероводорода, угольной, серной и органических (жирных и ароматических) кислот, фенолов, индола, скатола и др. тел. Вода, щелочи и кислоты также способны при нагревании различным образом гидратировать белки, расщепляя их на тела отчасти такие же, отчасти подобные тем, которые происходят при гниении.
Реакции Гидратация 2 и 3 группы протекают по большей части медленно, не обнаруживая значительных тепловых явлений. Что касается роли третьего вещества при них, то она может быть троякой. Гидратирующее вещество реагирует с одним из продуктов Гидратация, вступая с ним в соединение, напр., щелочь с кислотой, образующейся при омылении эфиров, или минеральная кислота с аммиаком при распадении амидов. Гидратирующее вещество, само оставаясь в конце превращения неизмененным, тем не менее принимает непосредственное участие в реакции, как, напр., серная кислота при Гидратация этилена, выражающейся след. 2 уравнениями:
CH2.CH2 + H(HSO4) = CH3.CH2(HSO4)
и
СН 3.СН 2 (НSО 4) + Н 2 O = СН 3.СН 2 (НО) + H(HSO 4).
Наконец, оно может действовать контактом (см). Таково, по-видимому, действие диастаза и слабых кислот на глюкозиды и углеводы и пепсина на белки.
П. П. Рубцов. Δ.
|
Смотрии так же... |
|