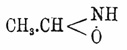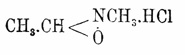Ацетальдоксим
Энциклопедия Брокгауза Ф.А. и Ефрона И.А. (1890 - 1916гг.) Статьи для написания рефератов, курсовых работ, научные статьи, биографии (118447 статей и 6000 рисунков).
|
|
| А | Б | В | Г | Д | Е | Ё | Ж | З | И | Й | К | Л | М | Н | О | П | Р | С | Т | У | Ф | Х | Ц | Ч | Ш | Щ | Ы | Э | Ю | Я | A | B | C | D | E | F | G | H | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | Z |
| А | АА | АБ | АВ | АГ | АД | АЕ | АЖ | АЗ | АИ | АЙ | АК | АЛ | АМ | АН | АО | АП | АР | АС | АТ | АУ | АФ | АХ | АЦ | АЧ | АШ | АЩ | АЭ | АЮ | АЯ |
| АЦЕ |
| АЦИ |
| АЦТ |
| АЦУ |
| АЦХ |
Ацетальдоксим CH3.CH:N.OH, или
(см. Альдоксимы и Изонитрозосоединения) существует в форме двух изомеров (Дёнстен и Даймонд, 1892 г.), которые, однако, не соответствуют двум приведенным формулам, а являются, по-видимому, стабильной и лабильной формой 1-й формулы. Твердый α - Ацетальдоксим, плав. при 47° и при нагревании до 100° — 115° переходит в β - A. с темп. плавл. 13°. Последний, однако, неоднороден и представляет раствор стабильной формы (α) Ацетальдоксим в жидкой лабильной (β) форме Ацетальдоксим Наблюдение упругости пара жидкого и твердого (α) Ацетальдоксим показали, что ниже 13° упругость пара жидкого Ацетальдоксим выше упругости пара кристаллического Ацетальдоксим; выше 13° — наоборот. Определение молекулярного веса по Раулю в уксуснокислом растворе дало для обеих форм величины, отвечающие формуле С 2 Н 5 NО. Темп. кипения Ацетальдоксим — 114° — 115°. Продукты присоединения галоидалкилов к Ацетальдоксим (Дёнстен и Гульдинг, 1897) имеют основные свойства; соли их при гидролизе распадаются на альдегид и β - алкилгидроксиламин, почему им придают строение 2-й из написанных
выше формул Ацетальдоксим, напр.:
При окислении Ацетальдоксим реактивом Каро [160 г персульфата калия растворяют в 180 г конц. H 2SO4, прибавляют 400 г льда и 450 г поташа.] получается ацетгидроксамовая кисл. CH 3.C(OH):N.OH, изонитроэтан и нитроэтан (Бамбергер, 1900). С хлористым ацетилом и уксусным ангидридом, по Дёнстену, как α - Ацетальдоксим, так и β -A. дают на холоду ацетильные производные, при нагревании — ацетонитрил.
П. Гр.
|
Смотрии так же... |
|