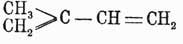|
Иллюстрация к статье на тему "Углеводороды ацетиленовые". Статьи для написания рефератов, курсовых работ, научные статьи, биографии, очерки, аннотации, описания.
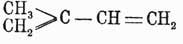
Углеводороды ацетиленовые - — Под этим названием подразумевают непредельные Углеводороды ацетиленовые формулы C nH2n—2, представителем которых являлся с давних пор ацетилен C 2H2 (см. Ацетилен и Углеродистый кальций). В настоящее время Углеводороды ацетиленовые формулы C nH2n—2 можно подразделить на следующие виды: а) собственно ацетиленовые Углеводороды ацетиленовые, b) алленовые Углеводороды ацетиленовые и с) диэтиленовые Углеводороды ацетиленовые а) Ацетиленовые Углеводороды ацетиленовые могут быть произведены из ацетилена, замещая в нем атомы водорода различными спиртовыми радикалами. В ацетилене, а также во всех ацетиленовых Углеводороды ацетиленовые мы имеем одну тройную связь между двумя углеродными атомами, поэтому строение (см.) ацетилена есть НС≡СН, а замещая в нем или один, или оба атома водорода углеводородными радикалами, мы получим две группы ацетиленовых Углеводороды ацетиленовые: 1) однозамещенные ацетилены R—С≡СН и 2) двузамещенные ацетилены R—С≡С—R', где R и R' суть CH 3, C2H5 и т. д. Все эти Углеводороды ацетиленовые называются так, что к слову ацетилен прибавляют названия радикалов, напр., метилацетилен (он же аллилен, пропин), диметилацетилен (2-бутин, кротониден) и т. д. Однозамещенные ацетилены, как видно из формулы их строения, имеют еще один ацетиленовый водород и потому способны давать металлические производные R—C≡CAg и (R—C≡C)Cu 2 при действии на них аммиачных растворов азотнокислого серебра или полухлористой меди; из этих соединений при действии минеральных кислот снова получаются первоначальные Углеводороды ацетиленовые Эта реакция позволяет отличать однозамещенные ацетилены от остальных видов Углеводороды ацетиленовые ряда C nH2n—2. Однозамещенные ацетилены получаются: 1) действием спиртовой щелочи на однозамещенные бромистые этилены (Савич, Марковников, Флавицкий, Крылов и Эльтеков): R—CHBr—CH2Br — 2HBr = R—C≡CH. 2) действием спиртовой щелочи на хлоропроизводные альдегидов с первичными радикалами в составе и 3) действием спиртовой щелочи на хлоропроизводные кетонов, которые содержат в своем составе радикал метил (Брюльянтс, Фридель): R—CCl2—СН3—2НСl = R—C≡СН. Сам ацетилен в настоящее время добывается в больших количествах действием воды на углеродистый кальций (см.): C 2 Ca + 2Н 2 О = С 2 Н 2 + Ca(ОН) 2. Однозамещенные ацетилены по своим химическим свойствам походят на ацетилен. Они способны на реакцию присоединения галоидов и галоидоводородных кислот; под влиянием серной кислоты, сулемы и бромной ртути они присоединяют воду и дают кетоны (Альмединген, Кучеров, Крылов, Флавицкий, Бегаль): R—C≡СH + Н 2 О = R—СО—СН 3. Однозамещенные ацетилены присоединяют хлорноватистую и бромноватистую кислоты и дают несимметричные дихлор- и дибромацетоны (Витторф), напр.: R—C≡CH + 2HClO = R—CO—CHCl 2 + Н 2 О. При нагревании однозамещенных ацетиленов со спиртовой щелочью в запаянных трубках при 170° происходит изомерное превращение их в двузамещенные ацетилены (Фаворский). Эта изомеризация может быть объяснена присоединением элементов этильного спирта (вернее, С 2 Н 5 ОК) и затем снова их отщеплением в другом направлении. Однозамещенные ацетилены с первичным радикалом в составе превращаются в двузамещенные ацетилены: СН 3 —СH 2 —С≡СН = СН 3 —С≡С—СН 3; однозамещенные ацетилены со вторичным радикалом превращаются в гем-двузамещенные аллены: (CH 3)2 —CH—С≡СН = (СН 3)2 С=С=CH 2, и, наконец, однозамещенные ацетилены с третичным радикалом, напр. (СН 3)3 C—С≡СН, вовсе не претерпевают изомерного превращения. Двузамещенные ацетилены R—С≡С—R' содержат два радикала и не имеют более ацетиленового водорода и потому не дают металлических производных. Они получаются: 1) действием спиртового раствора едкого кали на такие предельные кетонные двухлорпроизводные, которые в соседстве с C, связанным с хлором, не содержат радикала метила, напр.: СН 3 —СН 2 —СCl 2 —СН 2 —СН 3 + 2КОН = СН 3 —СН 2 —С≡C—CH 3 + 2KCl + 2H2 O; 2) при действии спиртовой щелочи на некоторые предельные двугалоидопроизводные, у которых атомы галоида находятся у разных С (Эльтеков), напр.: СН 3 —CHBr—CHBr—СН 3 + 2КНО = CH 3 —С≡С—СН 3 + 2KBr + 2Н 2 О; 3) изомеризацией под влиянием спиртовой щелочи однозамещенных ацетиленов (Фаворский), см. выше. По некоторым своим химическим свойствам эти Углеводороды ацетиленовые сходны с однозамещенными; так, под влиянием разведенной серной кислоты они гидратируются и превращаются в кетоны: CH 3C≡CCH3 + Н 2 О = CH 3—CH2—CO—CH3; при действии крепкой серной кислоты они полимеризуются в Углеводороды ацетиленовые бензольного ряда, напр.: 3CH 3—C≡C—CH3 = C6(CH3)6 (гексаметилбензол). Двузамещенные ацетилены при нагревании с металлическим натрием способны претерпевать изомерное превращение и переходят в однозамещенные ацетилены (Фаворский), напр. для этилметилацетилена (пентина): 2CH 3—CH2—C≡C—CH3 + 2Na = 2CH3—CH2—CH2 —C≡CNa, получается натриевое производное пропилацетилена, которое при действии воды и спирта превращается в пропилацетилен (4-пентин); это натриевое производное в присутствии эфира при действии на него угольного ангидрида превращается в ацетиленкарбоновую кислоту CH 3—CH2—CH2 —C≡COOH. Двузамещенные ацетилены присоединяют хлорноватистую кислоту и дают несимметричные дихлоркетоны (Фаворский). Так, диметилацетилен дает дихорэтилметилкетон: CH 3—C≡C—CH3 + 2HClO = CH3—CCl2—CO—CH3; эти дихлоркетоны под влиянием щелочи переходят в кислоты акрилового ряда. Двузамещенные ацетилены присоединяют к себе галоиды и галоидоводородные кислоты, причем следует заметить, что главным образом присоединяется одна частица галоидоводородных кислот и в результате получается непредельный бромюр (Ипатьев): R—C≡C—R + HBr = R—C H=CHBr—CH3. Одно- и двузамещенные ацетиленовые Углеводороды ацетиленовые представляют жидкости, для низших членов ряда очень легколетучие (аллилен при обыкн. условиях — газ), перегоняющиеся без разложения. Уд. вес их относительно весьма велик, а удельные объемы еще менее, чем у этиленовых Углеводороды ацетиленовые Нахождение в их частицах тройной связи сказывается на величине их частичного светопреломления; тройная углеродная связь увеличивает частичное преломление на величину около 2, которая, следовательно, близка к величине, вызываемой двойной связью. b) Алленовые Углеводороды ацетиленовые могут быть образованы из углеводорода аллена C3H4, который является их простейшим представителем. В алленовых Углеводороды ацетиленовые имеется две двойные связи, которые находятся по соседству; строение аллена будет: H 2C=C=CH2; другие алленовые Углеводороды ацетиленовые могут быть выведены из аллена, если замещать атомы водорода углеводородными радикалами, и потому гомологи аллена могут быть разделены на моно-, дву-, трех- и четырехзамещенные аллены, причем двузамещенные аллены могут быть симметричные и несимметричные, в последнем случае оба радикала будут замещать оба атома водорода при одном и том же углеродном атоме. Аллен получается электролизом итаконовой кислоты: СН 2 =С(СО 2 Н)—СН 2 (СО 2 Н) = СН 2 =С=CH 2 + 2CO2 + H2; более удобно его добывать по способу Густавсона и Демьянова из трибромгидрина глицерина, от которого сначала отнимают частицу бромистого водорода едким кали и на полученный дибромгидрин глицида действуют цинковой пылью в присутствии спирта: CH 2=CBr—CH2Br + Zn = CH2=C=CH2 + ZnBr2. Алленовые Углеводороды ацетиленовые могут получаться следующими реакциями. 1) Изомерным превращением однозамещенных ацетиленов с вторичным радикалом в составе (Фаворский). 2) Действием спиртовой щелочи на дибромиды, полученные действием брома на третичные спирты, при чем получаются двух- или трехзамещенные аллены в зависимости от строения радикалов, входящих в состав третичного спирта (Ипатьев); так, напр.: (СН 3)2 Br—СНBr—СН 3 — 2HBr = (СН 3)2 С=С=CH 3 (гем-диметилаллен, валерилен); (CH 3)2—CBr—CHBr—CH2—CH3 — 2HBr = (CH3)2C=C=CH—CH3 (триметилаллен). 2) Действием спиртовой щелочи на хлорюры гем-двузамещенных ацетонов при 150°—170° получаются гем-двузамещенные аллены (Ипатьев); так, напр.: (CH 3)—CCl2—CH(C2H5)2 — 2HCl = CH2=C=C(C2H5)2. В настоящее время не все виды алленовых углеводородов известны. До сих пор не получено ни одного симметрично двузамещенного аллена, и при существующих способах добывания Углеводороды ацетиленовые ряда C nH2n—2 образования трудно ожидать, если установившиеся воззрения относительно устойчивости углеводородных частиц отвечают действительности. Точно так же является сомнение в том, что единственный известный четырехзамещенный аллен, тетраметилаллен (Анри), принадлежит к классу алленов. Относительно реакций, которые изучены с алленовыми Углеводороды ацетиленовые, то число их очень ограничено. При нагревании они способны сравнительно легко уплотняться и, по-видимому, переходят в терпены. Триметилаллен и другие, вероятно, трехзамещенные аллены не изомеризуются под влиянием спиртовой щелочи в двузамещенные ацетилены (Ипатьев). Аллены соединяются с бромом, но присоединить к ним 4 атома брома не удается. Наиболее всего изучена реакция присоединения бромистого водорода в уксуснокислом растворе к алленам. Эта реакция позволяет отличить алленовый Углеводороды ацетиленовые от двузамещенного ацетилена и, кроме того, дает возможность по характеру полученного дибромида определить, к которому виду алленов относится исследуемый Углеводороды ацетиленовые (Ипатьев). Гем-двузамещенные аллены при присоединении двух частиц бромистого водорода дают бромистые гем-двузамещенные триметилены: R 2C=C=CH2 + 2HBr = R2CBr—CH2—CH2 Br, которые при действии спиртовой щелочи в колбе с обратно поставленным холодильником дают непредельные первичные гем-двузамещенные аллилэтиловые эфиры и двойная связь у которых находится между вторичным и третичным С, вследствие чего образуется кристаллический хлорооксим от присоединения хлористого нитрозила:
|