|
Иллюстрация к статье на тему "Сероуглерод*". Статьи для написания рефератов, курсовых работ, научные статьи, биографии, очерки, аннотации, описания.
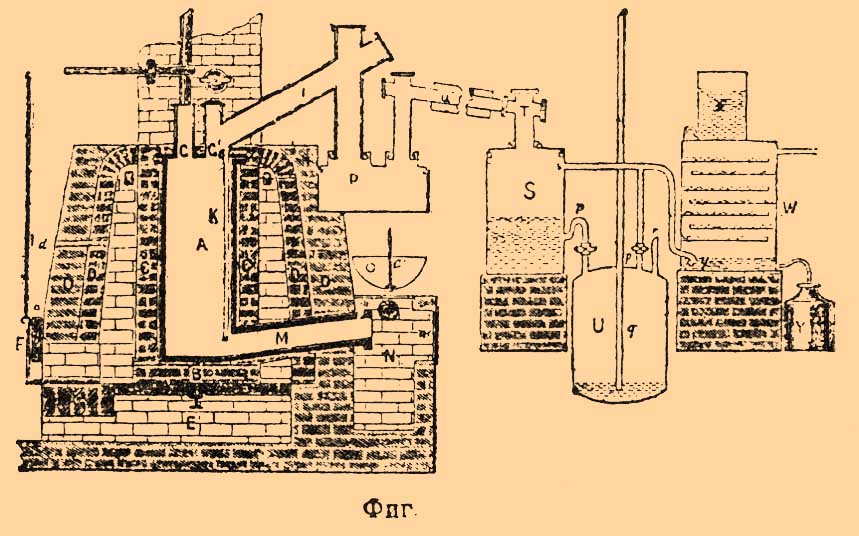
Сероуглерод* - CS2 (сернистый углерод, хим.-техн.) — Сероуглерод* открыт Лампадиусом в 1796 г.; он представляет бесцветную, легкоподвижную жидкость с приятным эфирным запахом, когда он чист; уд. в. его при 0° — 1,2922; 15° — 1,2708; 20° — 1,2636; при темп. кип. — 1,2233 (уд. веса отнесены к воде при 4°); темп. кип. 46,5—46,8°; критич. темп. 196,2°, теплоемкость 0,2179 (между 5° и 10°) и 0,2206 (между 15° и 20°); скрытая теплота испарения 90 кал. при 0° и 86,7 при темп. кип. Сероуглерод* затвердевает около —116°; обладает большим показателем преломления, именно 1,65234 для фрауэнгоферовой линии F и 1,61736 для линии С; мало растворим в воде; растворимость его уменьшается с температурой, напр., в 1 литре воды при 0° растворяется 2,04 г Сероуглерод*, при 10° — 1,94; при 20° — 1,79; при 30° — 155; 40° — 1,11; 49° — 0,14 г (Пармантье и Шансель). Вода, насыщенная Сероуглерод*, имеет антисептические свойства. С абсолютным спиртом Сероуглерод* смешивается во всех пропорциях; водный же спирт растворяет его до известного предела и тем меньше, чем больше спирт содержит воды (на этом был основан один из способов для определения крепости спирта). Сероуглерод* легко растворяется в эфире и жирных маслах. Он растворяет серу, фосфор, бром, йод, каучук, гуттаперчу, смолы, жиры, сероводород, сернистую кислоту, окислы азота и проч. Сероуглерод медленно разлагается при хранении, в особенности при действии света и воды; при этом выделяется красно-бурое вещество, вероятно, CS. При пропускании через накаленную трубку Сероуглерод* разлагается постепенно на уголь и серу, причем устанавливается известное равновесие, так как в этих же условиях происходит образование CS 2 соединением углерода с серой. Соединение это происходит с поглощением тепла (26 б. кал. на молекулу); этим и объясняется сравнительно легкое распадение Сероуглерод* на свои составные части; напр. при взрыве гремучей ртути в парах Сероуглерод* он распадается на серу и уголь, который выделяется в мелкораздробленном состоянии. Сероуглерод* очень легко воспламеняется — по Бертело, даже легче эфира; при горении выделяется большое количество тепла (3,49 б. кал. на 1 г CS 2); в смеси с кислородом пары Сероуглерод* сгорают со взрывом. Азотная кислота при обыкн. темп. не действует на Сероуглерод*; при взбалтывании Сероуглерод* с дымящейся азотной кислотой он извлекает растворенный в ней азотноватый ангидрид NO 2. Смесь Сероуглерод* с NO 2 образует взрывчатое вещество, так наз. панкластит; серная кислота разлагает Сероуглерод* Сероуглерод* способен соединяться со щелочами, сернистыми металлами и аминами, образуя различные тиосоединения. Он вредно действует на организм; при вдыхании производит головную боль, рвоту и вызывает общее угнетенное состояние, меланхолию, сопровождающуюся притуплением памяти и половым бессилием; поэтому при фабрикации и применении Сероуглерод* должны быть приняты все меры, чтобы предохранить рабочих от отравления парами Сероуглерод*
|
