|
Иллюстрация к статье на тему "Правило фаз*". Статьи для написания рефератов, курсовых работ, научные статьи, биографии, очерки, аннотации, описания.
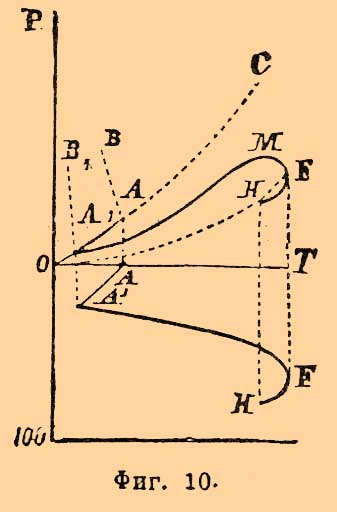
Правило фаз* - (хим.) — неоднородность любой химической системы, находящейся в равновесии, может обуславливаться только одновременным присутствием в ней различных однородных тел, взаимно соприкасающихся; таков, напр., случай твердой соли и находящегося над ней насыщенного раствора и т. д. Отдельные, однородные тела, из которых сложена система, могут быть в газообразном, жидком или твердом состояниях; число твердых тел и число взаимно не растворяющихся жидкостей, которые принимают участие в равновесии, не подлежит какому-либо ограничению; что касается паро- или газообразных тел, то благодаря способности их смешиваться во всех отношениях, паро- или газообразный комплекс, входящий в систему, должен быть всегда в единственном числе. Гиббс предложил называть фазами те физически и химически одпородные массы (иначе, массы однородной концентрации), из которых сложена данная неоднородная равновесная система. Фазами могут быть потому и физич. смеси, и химически однородные тела; число их, следовательно, не всегда совпадает с числом химических тел, которые могут быть выделены из данной системы; так, всякий раствор, будет ли он твердый (см. Растворы), жидкий или газообразный, представляет собой отдельную фазу, за химические же тела (простые или сложные), ее образующие, мы должны принимать исключительно те, концентрация которых может быть произвольно изменена. Напр., при рассмотрении равновесия между углекальциевой солью, окисью кальция и углекислым газом, за тела, слагающие данную систему мы должны принять СО 2 и СаО, потому что их концентрация может быть произвольно изменяема и их двух вполне достаточно для образования всех тут возможных равновесных систем (ср., что сказано ниже при двух реагирующих телах); нельзя принять за слагающие сами элементы кальций, кислород и углерод, так как они не представляют независимых переменных и, что не менее важно — не находятся в равновесии с данной системой [Paзличиe числа не зависимых друг от друга тел, образующих данную равновесную систему, от числа химических индивидуумов, в ней могущих содержаться, еще яснее выступает на следующем примере. Положим, что в воде растворены одновременно хлористый калий и бромистый натрий, в силу двойного разложения они дадут некоторые количества бромистого калия и хлористого натрия. Нетрудно убедиться, что несмотря на присутствие четырех солей, мы имеем дело всего с тремя независимыми переменными (предполагая концентрацию первоначально взятых солей определенной). Действительно, представим себе, что количества КСl, КВr и NaCl нами установлены, количество неизмененного NaBr, очевидно, будет тем самым косвенно определено; оно не является, следовательно, независимым. К тому же заключению приводит и то соображение, что достаточно в данном случае трех аналитических данных (напр., определений количеств K, Cl, Br), чтобы иметь возможность вычислить четвертое неизвестное (содержание Na, Мейергоффер). Аналогичные соображения позволяют обходиться, не прибегая к теории электролитической диссоциации, при изложении с точки зрения Правило фаз* фаз случаев равновесия водных растворов солей (Банкрофт).]. Гиббсу (Gibbs) принадлежит положение, что в системах, находящихся под равномерным влиянием тяготения, электрического, капиллярного или какого-либо иного натяжения, — состояние фаз определяется: давлением и температурой системы и химическими потенциалами тел, из которых она (система) сложена. При равновесии — потенциал данного тела, находящегося в различных фазах, обладает определенной постоянной величиной, и потому: 1) для любой фазы мы можем составить уравнение, которое будет связывать эти величины между собой, и 2) для каждой другой фазы, находящейся в равновесии с первой, будем иметь такого же вида уравнение, содержащее те же переменные. Несмотря на то, что неизвестны ни эти отдельные уравнения, ни химические потенциалы участвующих в данной системе тел, все же эти соображения позволили Гиббсу вывести вполне определенные заключения о характере и числе возможных случаев равновесия при неизвестном числе тел, участвующих в образовании системы. Действйтельно, число независимых переменных для n тел, по определению равно "n + 2" (n химических потенциалов + температура + давление), а следовательно, число теоретических уравнений равно числу переменных только при наличности "n + 2" фаз; это число фаз является, кроме того, максимальным для n не зависимых друг от друга химических тел. Только в этом случае все переменные имеют вполне определенное численное значение, иначе говоря, сосуществование "n + 2" фаз влечет за собой определенное соотношение между температурой и давлением; такие системы, не обладающие степенью свободы (Рике), Тревор называет безвариантными (nonvariant system). Если условиться откладывать температуры по оси абсцисс прамоугольных координат, а по оси ординат — давления, то в плоскости координат всегда можно найти такую точку, которая будет изображать состояние системы, сложенной из n тел и имеющей "n + 2" фаз; эту точку принято называть "инверсионной", или "точкой обращения" (Фан'т-Гофф). Когда при n реагирующих телах имеется налицо только "n + 1" фаз, то число неизвестных превышает на единицу число уравнений, которые можно для нее построить, и система оказывается обладающей одной степенью свободы, моновариантной (по Тревору — monovariant system); для такой системы величина одной из переменных, или температуры, или давления, может быть произвольно выбрана; ряду данных температур будут в ней отвечать вполне определенные давления, и наоборот, определенные давления возможны будут только при определенных температурах; в диаграмме температур и давлений такой системе будет отвечать уже не точка, а кривая линия. Если представить себе, что из сосуществующих при инверсионной точке "n + 2" фаз по очереди будет исчезать какая-нибудь из них, то, очевидно, мы получим в координатной плоскости "n + 2" кривых, которые все будут пересекаться при "точке обращения". Система из n тел, образованная n фазами, называется дивариантной (divariant system); две переменные могут быть в ней заранее выбраны, и в диаграмме температур и давлений такой системе отвечает определенная площадь, границы которой определяются кривыми моновариантных систем. В дивариантной системе при данной температуре можно иметь (при соответственных изменениях концентраций) целый ряд давлений; при данном давлении температура может меняться в зависимости от концентрации, или наоборот, концентрация может меняться с изменением температуры и т. д. Наконец, системы из n слагаемых (реагирующих тел), состоящия из n — 1, n — 2 и т. д. фаз называются три-, тетравариантными и т. д. (trivariant, tetravariant system); число степеней свободы, очевидно, возрастает по мере увеличения числа реагирующих тел, сравнительно с числом фаз; на практике иcследование три- и т. д. вариантных систем не представляет интереса благодаря их малой определенности и слишком большому числу возможных комбинаций. Системы, обнимаемые Правило фаз* фаз, подчинены, как равновесные, общему закону Ле-Шателье, по которому, "всякие изменения внешних факторов равновесия влекут за собой обратные изменения внутри системы" (см. Обратимость химических реакций), а именно: 1) нарастание температуры вызывает в системе превращение, стремящееся понизить температуру, поглощающее, следовательно, тепло, и обратно, и 2) всякое увеличение внешнего давления вызывает такое перемещение равновесия, которое влечет за собой понижение давления, состоящее, следовательно, в уменьшении объема системы, и обратно. Следующие частные случаи наглядно поясняют вышеизложенное.
|
