|
Иллюстрация к статье на тему "Марганец, химический элемент". Статьи для написания рефератов, курсовых работ, научные статьи, биографии, очерки, аннотации, описания.
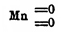
Марганец, химический элемент - (Manganè se — франц. и англ.; Mangan — нем.; Mn = 55,09 [Среднее из 55,16 (Dewar и Scott, 1883) и 55,02 (Marimac, 1884)]. Уже древние знали о существовании главной руды Марганец, пиролюзита, употребляли этот минерал при приготовлении стекла (Плиний Ст.) и уподобляли его магнитному железняку, хотя и знали, что он железа не притягивает. Шееле, в своей статье "De magnesia nigra" (1774), положил начало изучению M., а вместе с тем и хлора, кислорода и бария (в им исследованном материале присутствовала и ВаО). В том же году был получен и металлический Марганец Ганом. Кроме magnesia nigra существовало (XVI в.) название того же минерала — lapis manganensis; отсюда и ведет свое начало современное наименование металла. Соединения Марганец очень распространены в природе, но обыкновенно в малых количествах. Богатые металлом руды и минералы сдедующие: пиролюзит MnО 2, браунит Mn2O3, гаусманнит Mn3O4, псиломелан (Mn, Ва)О.MnО 2, манганит Mn2O2(OH)2, марганцевый шпат MnСО 3 обыкновенно в изоморфных смешениях (Mn,Fe)CO 3, (Mn,Ca,Mg)CO3, родонит MnSiO3. В малых количествах Марганец находится в большинстве силикатов, а потому присутствует в почвах, находится в золе растений и в костях животных. Встречается в виде сернистых соединений MnS и MnS 2, a также образует изоморфные смешения с другими сернистыми металлами. В самородном виде не встречается, потому что очень легко окисляется и труднее железа восстанавливается. Существует несколько путей для получения металлического Марганец: через восстановление углем окислов при сильном калении (John, Deville, Moissan), при сплавлении MnCl 2 с CaF 2 и металлич. Na (Brunner), путем электролиза крепкого раствора MnCl 2 (Bunsen). M. обыкновенно не получается чистым, содержит углерод, кремний. В чистом виде получают из амальгамы; амальгаму же можно получить, действуя амальгамой натрия на раствор MnCl 2, или электролизом того же раствора, употребляя катод из ртути; по полной отгонке ртути, что совершается при 440° (Moissan), остается порошкообразный металл. Водород и окись углерода более или менее легко действуют на многочисленные окислы Марганец, за исключением закиси MnО; ее они не восстанавливают даже при 600° (Wright и Luff), а потому все они водородом превращаются в MnО; последняя при сплавлении с металлическим алюминием, под известью и плавиковым шпатом, дает довольно чистый металл (до 97% — Greene и Wahl, 1893); при действии магния на сплав MnCl 2 + КСl 2 (1 в. ч. + 2 в. ч.) получается королек очень чистого металла (Glatzel, 1889), удел. вес которого, d 20°/20° = 7,3921. По цвету Марганец приближается к железу, но обладает красноватым отливом, подобно висмуту; ломок и очень тверд — режет сталь, стекло; совершенно не притягивается магнитом, если не содержит железа; теплоемкость 0,1217 (с содерж. Si, при 14° — 97°, Regnault); плавится труднее железа, при 1900°; по-видимому, летуч при температурах немного высших точки плавления [Как показали опыты нагревания до белого каления в фарфоровой трубке в струе окиси углерода, водорода или азота (Lorenz и Heusler, 1892). Ни с H, ни с CO не получается при этом летучего соединения, подобного NiC 4O4, как показало спектроскопическое исследование пламени H или СО, зажженных при выходе из трубки]. Марганец легко выделяет водород с разведенными кислотами, при чем получаются соли закиси MnХ 2; даже на подогретую воду он действует и окисляется при обыкновенной температуры на воздухе. Порошкообразный Марганец, из амальгамы, еще легче окисляется на воздухе и под водой; при взбалтывании его с водой и воздухом получается перекись водорода. Сплавы марганца с железом указаны ниже в ст. Марганец (металлургия), марганцевая сталь, ферроманган, белый чугун. Сплавы с медью очень похожи на сплавы олова с медью (см. Манганин). Сплав Марганец (80%) с цинком (5%) и медью (15%), так назыв. марганцевый нейзильбер, получается при восстановлении углем окислов, белого цвета, легко обрабатывается и хорошо полируется. О марганцовой бронзе см. Бронза. Из жидкой амальгамы отжиманием получена кристаллическая MnHg 5 [О. Prelingep (1893). Жидкая амальгама была получена, по Муассану, электролизом, по отгонке всей ртути в струе водорода при темно-красном калении остался серый пористый Марганец, уд. в. 7,4212, такой Марганец реагирует с азотной кислотой с воспламенением, из нашатырного раствора выделяет аммиак и водород, а также следующие металлы из их соляных растворов — Sn, Рb, Sb, As, Bi, Сr, Fe, Со, Ni, Сu, Zu и Cd]. Спектр Марганец дают искры от вторичной спирали, полученные на поверхности раствора MnCl 2, или свет дуги между электродами из металлического Марганец Спектр содержит много линий: в оранжевой части (3 л.), в синей (5 л.), в фиолетовой (2 л.). Спектр от MnO — полосчатый; источником служит огонь при бессемеровском процессе.
|