|
Иллюстрация к статье на тему "Кислород". Статьи для написания рефератов, курсовых работ, научные статьи, биографии, очерки, аннотации, описания.
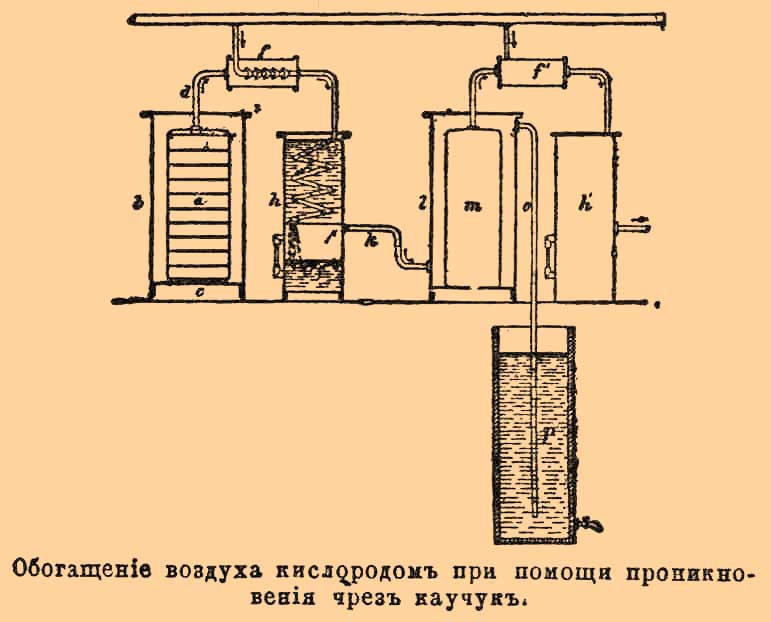
Кислород - (нем. Sauerstoff, франц. oxyg è ne, англ. oxygen) — нормальная и весьма важная составная часть воздуха, в обычных условиях температуры и давления бесцветный газ, без вкуса и запаха (история открытия Кислород — см. Воздух). В виде соединений Кислород распространен на земной поверхности так, как никакой другой элемент. Он составляет 8/9 весовых частей воды, которая, в свою очередь, занимает почти 3/4 земной поверхности. Большинство горных пород и земель состоит из соединений Кислород, причем содержание его в некоторых из них доходит до 53% (песок, кварц), вообще же можно считать содержание в них Кислород до 1/3 их веса. Организмы также богаты им: так, растения, помимо Кислород воды, содержат его до 40% в виде других соединений, а животные до 20% своего веса. Несмотря на громадное распространение на земной поверхности, несмотря на большое сродство ко всем телам (Кислород соединяется прямо или косвенно со всеми элементами, за исключением фтора, с которым неизвестно соединений), Кислород остался еще в свободном состоянии и в смеси с азотом образовал атмосферный воздух. В воздухе он содержится в количестве около 1/4 по весу или около 1/5 по объему и весит примерно около 122x10 15 пудов, но это число, несмотря на свою чудовищность, ничтожно с тем количеством его, которое содержится в земной коре, хотя (по Менделееву) внутри земли содержание Кислород меньше, чем на поверхности. Что касается до внеземного распространения Кислород, то его еще не найдено; по новейшим спектроскопическим исследованиям Янсена, произведенным на вершине Монблана, на Солнце его не оказалось, следовательно, на Солнце он не находится в известной для нас форме, дающей определенный ряд спектральных линий. Нахождение кислорода на других планетах — см. Воздух. Роль кислорода в экономии природы также громадна, как и его распространение. Без него немыслимы такие процессы огромной важности, как дыхание, горение и гниение (см.). Первым из этих процессов обуславливается жизнь со всеми ее проявлениями, второй дает нам тепло, а вместе с тем энергию, необходимую для всякой механической работы; гниение же в связи с брожением доканчивает дело смерти, разрушая отжившие тела и превращая их главным образом в углекислоту и воду, которые снова идут на дело жизни. Помимо этих процессов, есть еще много других, которые обусловлены Кислород и известны под общим именем окисления. По своим физическим свойствам Кислород, как сказано, является бесцветным газом без запаха и вкуса. Плотность его относительно воздуха и вес литра — см. Воздух; абсолютный коэффициент преломления при 0° и 760 мм давления — 1,000271, относительный (к воздуху=1 при 0°) — 0,9245 (Маскар), т. е. меньше воздуха. Спектр поглощения Кислород — см. Воздух. Теплоемкость при постоянном давлении 0,2175, а при постоянном объеме 0,1550. Кислород плохой проводник тепла и электричества, но способен намагничиваться более, чем все другие газы, за исключением озона. Если магнитную силу железа обозначить через 1000000, то, по Беккерелю, для Кислород она выразится числом 377, а для воздуха — 88. При электролизе соединений Кислород он в виде газа всегда выделяется на положительном полюсе. Несмотря на многие попытки — Кислород долгое время не могли превратить в жидкость. Фарадею не удалось его сгустить при давлении 40 атмосфер и при температуре —110°. Попытки Андрюса и Наттерера также не увенчались успехом, хотя последний доводил давление до 1350 атм. Неудача происходила от того, что во всех этих опытах не достигалась критическая температура (см.) кислорода, т. е. та температура, выше которой газ никаким давлением не переводится в жидкое состояние. В 1877 году Кальете в Париже и Пикте в Женеве удалось, наконец, получить Кислород в жидком виде, но не удалось эту жидкость уединить, чего позднее достигли Вроблевский, Ольшевский, Дьюар и др., употребляя жидкий этилен и азот, причем температура доходит до —200°, поэтому не требуется больших давлений (см. Газы сжиженные).
|
