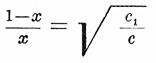|
Иллюстрация к статье на тему "Жадность". Статьи для написания рефератов, курсовых работ, научные статьи, биографии, очерки, аннотации, описания.
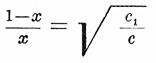
Жадность - (хим.; нем. Avidität) — термин, употребленный в первый раз Томсеном для обозначения стремления кислоты к нейтрализации основанием в сильно разбавленном водном растворе. Это есть коэффициент, показывающий распределение основания между двумя конкурирующими кислотами, взятыми в эквивалентных количествах. Если, например, Жадность серной кислоты относительно едкого натра, принимая Жадность соляной кислоты относительно того же основания за единицу, по определениям Томсена, равна 0, 4 9, а соответствующая величина для монохлоруксусной кислоты 0,09, то это значит, что реакция в эквивалентных количествах серной кислоты на монохлороуксуснонатриевую соль или, обратно, серно-натриевой соли на монохлоруксусную кислоту не пойдет до конца; в растворе установится равновесие, при котором распределение едкого натра таково, что на 0,49 весовых частей его в соединении с серной кислотой будет приходиться 0,09 весовых частей его в соединении с монохлоруксусной кислотой. Принимая за единицу все количество едкого натра, входящего в реакцию, а за x - количество его, соединившееся с монохлоруксусной кислотой, будем иметь в соединении с серной кислотой 1- x и, согласно жадностям указанных кислот, получим следующее соотношение: (1-x)/x=0,49/0,09, откуда x=155, или, другими словами, 15,5% едкого натра соединятся с монохлоруксусной, а остальные 84,5% — с серной кислотой. Определение Жадность кислот сводится к изучению распределения основания в водном растворе между двумя конкурирующими кислотами. О распределении же судят по изменению тех или иных физических свойств растворов, между которыми происходит взаимодействие. Такими физическими свойствами растворов являются теплота смешения (термохимический метод), удельный вес и обратная ему величина — удельный объем (объемно-химический метод), показатель преломления, вращение плоскости поляризации и т. п. Сущность подобных приемов состоит в определении величины данного свойства смеси растворов средней соли какой-нибудь кислоты с другой свободной кислотой в эквивалентных количествах. Отсюда, зная величину данного физического свойства для того случая, если бы реакция шла до конца, рассчитывается, какая доля наблюденного изменения этой величины обусловлена образованием средней соли одной и средней соли другой кислоты. Следующая таблица содержит величины жадностей некоторых кислот, определенные Оствальдом объемно-химическим путем (первый столбец) и Томсеном из измерений теплоты смешения (второй столбец).
|